原子结构与元素周期律
考纲再读
(1)了解元素、核素和同位素的含义。
(2)了解原子构成。了解原子序数、核电荷数、质子数、中子数、核外电子数以及它们之间的相互关系。。
(3)了解原子核外电子排布。
(4)掌握元素周期律的实质。了解元素周期表(长式)的结构(周期、族)及其应用。
(5)以第3周期为例,掌握同一周期内元素性质的递变规律与原子结构的关系。
(6)以IA和VIIA族为例,掌握同一主族内元素性质递变规律与原子结构的关系。
(7)了解金属、非金属在元素周期表中的位置及其性质递变的规律。
(8)了解化学键的定义。了解离子键、共价键的形成
主干知识整合
一、原子结构
1. 原子由原子核和核外电子构成;原子核由质子和中子构成;质子数决定核电荷数,核电荷数决定元素种类;质子数和中子数共同决定原子种类和质量数;由质量数可得近似相对原子质量;核外电子尤其是最外层电子数决定元素的化学性质;核外电子排布决定原子结构示意图。
2. 元素、核素、同位素
(1)元素:具有相同质子数的同一类原子的总称。包括质子数相同的各种原子或离子(游离态和化合态)
(2)核素:具有一定数目的质子和一定数目的中子的一种原子叫做核素。
(3)同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。
二、元素周期律和周期表
(1) 元素周期律是元素周期表的编排依据;元素周期表是元素周期律的具体表现形式。
(2) 元素周期律:随原子序数的递增,核电荷数递增:原子结构、原子半径、元素主要化合价、元素的金属性与非金属性呈周期性变化。
(3) 元素周期表:①排列顺序:最外电子层数相同的元素按原子序数递增顺序从左到右排成一横行;最外层电子数相同的元素按电子层数递增顺序从上到下排成一纵行。
②结构:七个周期(7个横行):三短(一、二、三周期);三长(四、五、六周期)一不全(第七周期为不完全周期);16个族(18个纵行)包括7个主族,7个副族,1个零族(稀有气体)和1个VIII族(8、9、10三个纵行)
③性质递变:同周期从左到右元素的金属性逐渐减弱,非金属性逐渐增强;同主族从上到下元素的金属性逐渐增强,非金属性逐渐减弱。
(4). 判断元素非金属性的强弱
①最高价氧化物对应水化物的酸性强弱
②与H2化合的难易及生成氢化物稳定性
③活泼非金属能置换出较不活泼非金属单质
④阴离子还原性强弱
⑤与变价金属反应产物中金属的价态
⑥电解时,在阳极先产生的为非金属性弱的单质
(5) 判断元素金属性的强弱
①最高价氧化物水化物碱性强弱
②与水或酸反应,置换出H2的难易
③活泼金属能从盐溶液中置换出不活泼金属
④阳离子氧化性强弱
⑤原电池中负极为活泼金属,正极为较不活泼金属
⑥电解时,在阴极先析出的为不活泼金属
⑦依据元素周期表,同周期从左到右金属性依次减弱,同主族从上到下依次增强
(6) 元素“位一构一性”之间的关系
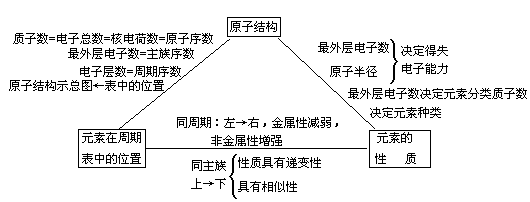
完整版资料请点击:原子结构与元素周期表
经营许可证编号:
京ICP备05067667号-32 | 京ICP证060601号|
京网文(2016)5762-750号 |
 京公网安备11010802021790号
京公网安备11010802021790号
Copyright 2011-2026 新东方教育科技集团有限公司, All Rights Reserved
新媒体平台资质审核电话:010-60908000-8941
考纲再读
(1)了解元素、核素和同位素的含义。
(2)了解原子构成。了解原子序数、核电荷数、质子数、中子数、核外电子数以及它们之间的相互关系。。
(3)了解原子核外电子排布。
(4)掌握元素周期律的实质。了解元素周期表(长式)的结构(周期、族)及其应用。
(5)以第3周期为例,掌握同一周期内元素性质的递变规律与原子结构的关系。
(6)以IA和VIIA族为例,掌握同一主族内元素性质递变规律与原子结构的关系。
(7)了解金属、非金属在元素周期表中的位置及其性质递变的规律。
(8)了解化学键的定义。了解离子键、共价键的形成
主干知识整合
一、原子结构
1. 原子由原子核和核外电子构成;原子核由质子和中子构成;质子数决定核电荷数,核电荷数决定元素种类;质子数和中子数共同决定原子种类和质量数;由质量数可得近似相对原子质量;核外电子尤其是最外层电子数决定元素的化学性质;核外电子排布决定原子结构示意图。
2. 元素、核素、同位素
(1)元素:具有相同质子数的同一类原子的总称。包括质子数相同的各种原子或离子(游离态和化合态)
(2)核素:具有一定数目的质子和一定数目的中子的一种原子叫做核素。
(3)同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。
二、元素周期律和周期表
(1) 元素周期律是元素周期表的编排依据;元素周期表是元素周期律的具体表现形式。
(2) 元素周期律:随原子序数的递增,核电荷数递增:原子结构、原子半径、元素主要化合价、元素的金属性与非金属性呈周期性变化。
(3) 元素周期表:①排列顺序:最外电子层数相同的元素按原子序数递增顺序从左到右排成一横行;最外层电子数相同的元素按电子层数递增顺序从上到下排成一纵行。
②结构:七个周期(7个横行):三短(一、二、三周期);三长(四、五、六周期)一不全(第七周期为不完全周期);16个族(18个纵行)包括7个主族,7个副族,1个零族(稀有气体)和1个VIII族(8、9、10三个纵行)
③性质递变:同周期从左到右元素的金属性逐渐减弱,非金属性逐渐增强;同主族从上到下元素的金属性逐渐增强,非金属性逐渐减弱。
(4). 判断元素非金属性的强弱
①最高价氧化物对应水化物的酸性强弱
②与H2化合的难易及生成氢化物稳定性
③活泼非金属能置换出较不活泼非金属单质
④阴离子还原性强弱
⑤与变价金属反应产物中金属的价态
⑥电解时,在阳极先产生的为非金属性弱的单质
(5) 判断元素金属性的强弱
①最高价氧化物水化物碱性强弱
②与水或酸反应,置换出H2的难易
③活泼金属能从盐溶液中置换出不活泼金属
④阳离子氧化性强弱
⑤原电池中负极为活泼金属,正极为较不活泼金属
⑥电解时,在阴极先析出的为不活泼金属
⑦依据元素周期表,同周期从左到右金属性依次减弱,同主族从上到下依次增强
(6) 元素“位一构一性”之间的关系

完整版资料请点击:原子结构与元素周期表