2019湖南高考化学知识点:热化学方程式的书写与判断
导读:在备考高考化学时,要时刻以课本为中心,以教学大纲和考试大纲为依据,明确复习要求,把握复习方向,全面回顾知识点,构建知识网络,良好的知识网络结构更利于学生认知结构的建构与优化。还要把握重难点,查缺补漏。以下是热化学方程式的书写与判断知识点汇总,供学生复习。
1.热化学方程式的书写步骤
步骤1 写方程——写出配平的化学方程式;
步骤2 标状态——用“s”、“l”、“g”、“aq”标明物质的聚集状态;
步骤3 标条件——标明反应物的温度和压强(101 kPa、25 ℃时可不标注);
步骤4 标ΔH——在方程式后写出ΔH,并根据信息注明ΔH的“+”或“−”;
步骤5 标数值——根据化学计量数计算写出ΔH的数值及单位。ΔH的单位一般为kJ·mol−1。
2.热化学方程式的判断
(1)检查是否标明聚集状态。
(2)检查ΔH的“+”“−”是否与吸热、放热一致。
(3)反应热ΔH的单位是否为“kJ·mol−1”。
(4)检查ΔH的数值是否与反应物或生成物的物质的量一致。
(5)表示燃烧热的热化学方程式,还要注意是否生成了稳定的氧化物。
书写热化学方程式的注意事项
(1)注意测定的条件:需注明反应热测定的温度和压强,如不注明条件,即指25℃,1.01×105 Pa。
(2)注意ΔH的标注:化学方程式的右边必须写上ΔH,若为吸热反应,ΔH为“+”,若为放热反应,ΔH为“−”,单位一般为kJ/mol或kJ·mol−1;根据焓的性质,若化学方程式中各物质的系数加倍,则ΔH的数值也加倍;若反应逆向进行,则ΔH改变符号,但绝对值不变。
(3)注意物质的聚集状态:反应热的数值和符号与反应物和生成物的聚集状态有关,因此必须注明物质的聚集状态(s、l、g、aq)才能完整地体现出热化学方程式的意义。热化学方程式中不需要标出“↑”和“↓”。
(4)注意化学计量数:热化学方程式中化学计量数表示参加反应的各物质的物质的量,可为整数或分数;而普通化学方程式中化学计量数宏观上表示各物质的物质的量,微观上表示原子分子数目,只能为整数,不能为分数。
(5)注意ΔH单位的意义:热化学方程式中,ΔH的单位为kJ·mol−1。这里的“mol−1”不表示具体物质,而是表示“1 mol反应”或“1 mol反应进度”,指“1 mol特定的反应组合”。如“H2(g)+ O2(g) H2O(1) ΔH=−285. 8 kJ·mol−1”,“1 mol反应”指“1 mol H2(g)与 mol O2(g)生成1 mol H2O(l)”这一特定反应组合。
(6)注意可逆反应ΔH的意义:不论化学反应是否可逆,热化学方程式中的ΔH都表示反应进行到底时的能量变化。
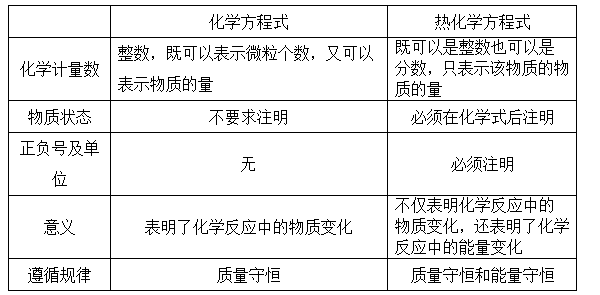
化学方程式与热化学方程式的比较
延伸阅读:
经营许可证编号:
京ICP备05067667号-32 | 京ICP证060601号|
京网文(2016)5762-750号 |
 京公网安备11010802021790号
京公网安备11010802021790号
Copyright 2011-2026 新东方教育科技集团有限公司, All Rights Reserved
新媒体平台资质审核电话:010-60908000-8941
导读:在备考高考化学时,要时刻以课本为中心,以教学大纲和考试大纲为依据,明确复习要求,把握复习方向,全面回顾知识点,构建知识网络,良好的知识网络结构更利于学生认知结构的建构与优化。还要把握重难点,查缺补漏。以下是热化学方程式的书写与判断知识点汇总,供学生复习。
1.热化学方程式的书写步骤
步骤1 写方程——写出配平的化学方程式;
步骤2 标状态——用“s”、“l”、“g”、“aq”标明物质的聚集状态;
步骤3 标条件——标明反应物的温度和压强(101 kPa、25 ℃时可不标注);
步骤4 标ΔH——在方程式后写出ΔH,并根据信息注明ΔH的“+”或“−”;
步骤5 标数值——根据化学计量数计算写出ΔH的数值及单位。ΔH的单位一般为kJ·mol−1。
2.热化学方程式的判断
(1)检查是否标明聚集状态。
(2)检查ΔH的“+”“−”是否与吸热、放热一致。
(3)反应热ΔH的单位是否为“kJ·mol−1”。
(4)检查ΔH的数值是否与反应物或生成物的物质的量一致。
(5)表示燃烧热的热化学方程式,还要注意是否生成了稳定的氧化物。
书写热化学方程式的注意事项
(1)注意测定的条件:需注明反应热测定的温度和压强,如不注明条件,即指25℃,1.01×105 Pa。
(2)注意ΔH的标注:化学方程式的右边必须写上ΔH,若为吸热反应,ΔH为“+”,若为放热反应,ΔH为“−”,单位一般为kJ/mol或kJ·mol−1;根据焓的性质,若化学方程式中各物质的系数加倍,则ΔH的数值也加倍;若反应逆向进行,则ΔH改变符号,但绝对值不变。
(3)注意物质的聚集状态:反应热的数值和符号与反应物和生成物的聚集状态有关,因此必须注明物质的聚集状态(s、l、g、aq)才能完整地体现出热化学方程式的意义。热化学方程式中不需要标出“↑”和“↓”。
(4)注意化学计量数:热化学方程式中化学计量数表示参加反应的各物质的物质的量,可为整数或分数;而普通化学方程式中化学计量数宏观上表示各物质的物质的量,微观上表示原子分子数目,只能为整数,不能为分数。
(5)注意ΔH单位的意义:热化学方程式中,ΔH的单位为kJ·mol−1。这里的“mol−1”不表示具体物质,而是表示“1 mol反应”或“1 mol反应进度”,指“1 mol特定的反应组合”。如“H2(g)+ O2(g) H2O(1) ΔH=−285. 8 kJ·mol−1”,“1 mol反应”指“1 mol H2(g)与 mol O2(g)生成1 mol H2O(l)”这一特定反应组合。
(6)注意可逆反应ΔH的意义:不论化学反应是否可逆,热化学方程式中的ΔH都表示反应进行到底时的能量变化。
化学方程式与热化学方程式的比较

延伸阅读: